中2理科「原子・分子と化学反応式」をまとめています。それに関連して、「物質をつくっているもの」、「化学式」、「単体と化合物」、「化学反応式」についてまとめています。
物質をつくっているもの
原子は、物質を作っている最小の粒。約100種類が知られています。
- 原子の大きさと質量…大きさ、質量ともにたいへん小さく、原子の種類ごとに異なる。(例)水素原子の直径は1cmの1億分の1。
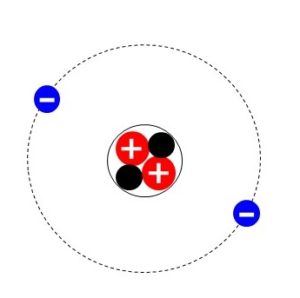
- 原子核…原子の中心にある
- 陽子…原子核の中には+の電気を帯びた粒子
- 中性子…電気を帯びていない粒子
- 電子…原子核のまわりを-の電気を帯びた粒子
原子の性質
- それ以上分けられない。
- なくなったり、新しくできたり、他の原子に変わったりしない。
- その種類ごとに質量が決まっている。
周期表
原子を質量の順に並べたとき、性質の似たものが周期的に現れる。こうした規則性をもとにつくった表。
分子
分子は、物質の性質を示す最小の粒子。原子が結びついてできた粒子で、結びついてる原子の種類と数によって物質の性質が決まる。分子をつくらない物質もある。
化学式
物質を原子の記号で表したもの.
- 分子からなる物質…酸素や水
- 分子をつくらない物質…銀、塩化ナトリウム
化学反応式
化学変化と状態変化は、物質が状態変化するときは、分子の集まり方が変わるだけで、物質の分子そのものは変わらない。
化学反応式とは、化学変化の様子を化学式で表した式。
- 酸化銀の熱分解 2Ag2O→4Ag+O2 (酸化銀→銀+酸素)
- 酸化銅 2Cu + O2 → 2CuO (銅+酸素→酸化銅
- 酸化マグネシウム 2Mg + O2 → 2MgO (マグネシウム+酸素→酸化マグネシウム)
- 水の分解 2H2O→2H2+O2 (水→水素+酸素)
- 酸化銅の還元 2CuO+C→2Cu+CO2
- 水酸化ナトリウムの熱分解 NaHCO3→Na2CO3+CO2+H2O
- 硫化鉄 Fe + S → FeS(鉄+硫黄→硫化鉄)
化合物
化合物は、2種類以上の元素から成り立っている純物質を、化合物という。化合物には、水、アンモニアなどのように分子から成り立っているものや食塩、水酸化ナトリウムのようにイオンから成り立っているものがある。
化合物と混合物の違い
化合物と混合物を混同することが多いので注意する。化合物はそれを構成する元素の性質とは異なる性質をもっている。例えば、水はそれを構成する酸素(気体)や水素(気体)の性質とはまったく異なる性質をもっている。
化合物と混合物を混同することが多いので注意する。化合物はそれを構成する元素の性質とは異なる性質をもっている。例えば、水はそれを構成する酸素(気体)や水素(気体)の性質とはまったく異なる性質をもっている。
それに対して、混合物は混合されている物質の性質を合わせ もつ。例えば、食塩水は塩辛いという食塩の性質と液体であるという水の性質をもつ。
単体
単体は、1種類の元素で成り立っている純物質を単体という。単体には、酸素、水素のように分子から成り立っているものや鉄、銀のように原子が集合して成り立っているものがある。


コメント