中1理科の「状態変化と温度」について、まとめています。「状態変化と温度」に関わる蒸発と沸騰についてと蒸留についてまとめています。それでは、中1理科の「状態変化と温度」をみていきましょう。
状態変化の要点
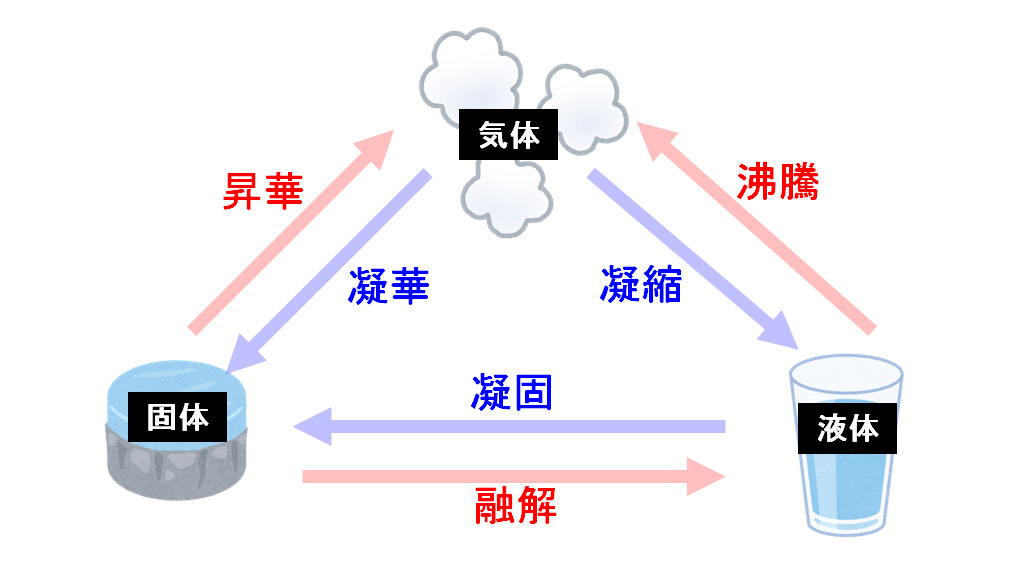
液体の表面で液体が気体に状態変化することを蒸発といいます。これに対して、液体の表面だけでなく液体の内部からも液体が気体に変わっていくことを沸騰といいます。加熱すると、固体→液体→気体の状態となるにつれて、構成する粒子の運動は激しくなる。
- 融点…固体が溶けて液体になるときの温度。(例)水=0℃、パルミチン酸=63℃、エタノール=-115℃。
- 沸点…液体が沸騰して気体になるときの温度。(例)水=100℃、パルチミン酸351℃、エタノール=78℃。
- 純粋な物質…1種類の物質からできているもの。(例)水、エタノール、パルミチン酸、塩化ナトリウム、鉄。
純粋な物質の融点や沸点は決まっているので、物質を見分ける手がかりとなります。状態変化してる間は、温度が一定になります。
- 混合物…いろいろな物質が混ざっているもの。(例)空気、食塩水、しょう油、みりん、ジュース、粘土。
混合物は、一定の融点や沸点を示されない、状態変化が起きている間も温度が変化します。
物質純粋な物質では、物質が状態変化するときの温度は決まっており、状態変化する間は温度が変わりません。
融点
固体の物質濃度上げたとき物質が液体になる温度。液体の物質の温度を下げた時。融点と同じ温度で物質が固体になる。
沸点
液体の物質の温度を上げたとき、物質が沸騰して気体になる温度。気体の物質の温度を下げた時、沸点と同じ温度で気体が物質が液体になる。
状態変化と体積の変化
一般に、固体→液体→気体と状態変化すると、体積はそのたびにだんだんに大きくなる。ただし、水の場合は例外で、固体→液体と状態変化すると体積が減少する。
- ロウなどの一般的な体積…固体<液体<気体と加熱すると大きくなる
- 水…液体(水)<固体(氷)<気体(水蒸気)と液体の水が一番小さい
一般に、固体→液体と変化する場合の体積変化より、液体→気体と変化する場合のほうが体積変化は大きい。例えば、水は,固体→液体の変化では体積が約10%減少するが、液体→気体の変化では、体積が約1700倍に増加する。
状態変化と密度の変化
状態変化によって、体積は変化するが、質量は変化しない。したがって、状態変化すると密度が変化することになる。一般的に、密度の値は、固体>液体>気体となるが、水の場合は、液体の状態がもっとも密度が大きい。
- ロウなどの一般的な密度…固体>液体>気体と固体が一番大きい
- 水…液体(水)>固体(氷)>気体(水蒸気)と液体の水が一番大きい
みりんを蒸留してエタノールを取り出す実験
<手順>
- 試験管にみりんをとり、弱火で加熱する。
- 3本の試験管アイウに液体を集める。
- 集めた液体を次のAからCのようにして調べる。
A…匂いを調べる
B…脱脂綿につけて、火をつける。
C…皮ふにをつける。
<結果>
試験管ア A(エタノールのにおい) B(長く燃える)C(冷たい感じがする)
試験管ウ A(においはしない)B(燃えない)C(ぬれて残る感じがする)
<考察>
加熱するとまずエタノールを多く含む気体が、次に水蒸気を多く含む気体が出てくる。
蒸留
蒸留は、液体を沸騰させて気体にし、それをまた液体にして集める方法。蒸留を利用すると、液体の混合物から沸点の違いによってそれぞれの物質を分けて取り出すことができる。みりんの実験では、エタノールの沸点が78℃で、水より低いため。初めに出てくる気体の中にエタノールが多く含まれている。
たとえば、沸点のちがいを利用して、混合物から純物質をとり出す実験操作で、加熱していくと、まず沸点が低い物質が気体となり、溶液から出ていく。これを冷却して、再び液体としてとり出すのである。食塩水を蒸留すれば、沸点の低い水が水蒸気となり、それを冷却して液体である水を得ることになる。
- 溶質…溶質は、水などの液体に溶けている物質。(例)砂糖、食塩、硝酸銅、エタノール、塩化水素。
- 溶媒…溶媒は、溶質を溶かしてる液体。(霊)水、エタノール。
- 溶液…溶液は、溶質が溶媒に溶けた液体。溶媒が水の溶液を特に水溶液といいます。
沸騰石
沸騰石は、くだいた素焼きなど沸騰石を入れないで加熱すると突沸とよばれる急激な沸騰現象が起こるので危険である。
温度計
純物質は決まった温度で沸騰するので、蒸留するときは、その蒸気の温度を測定する。温度が変化した場合は、そのときに気体となった物質に今までとは異なる物質が混入した可能性があると判断し、蒸留を中止する必要がある。このような理由があるので、蒸留を行う場合は、温度計を必ず用います。


コメント