中2理科「発熱反応と吸熱反応」についてまとめています。「発熱反応と吸熱反応」に関して、熱を発生する化学変化の実験、熱を吸収する化学変化の実験を通して学んでいきます。それでは、中2理科「発熱反応と吸熱反応」についてみていきましょう。
発熱反応
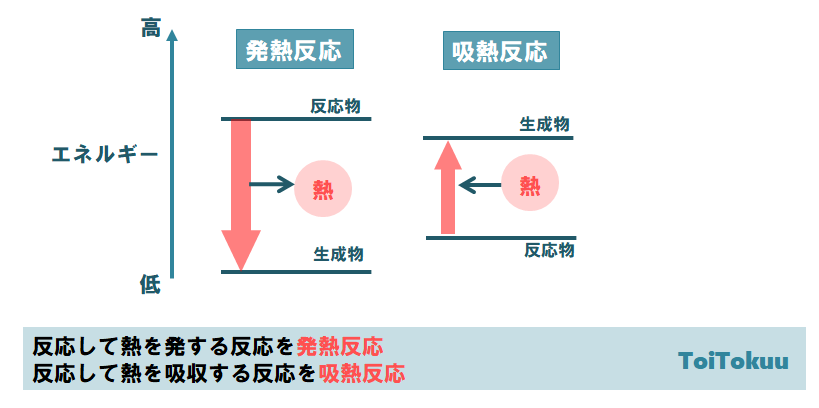
発熱反応とは、熱が発生する化学変化です。
燃焼
鉄やマグネシウムなどの金属の燃焼、有機物(水、アルコール、メタン、プロパンなど)の燃焼、炭(炭素)や水素などの燃焼。
化学かいろ
熱が空気中の酸素と化合して酸化鉄になるときに熱を発生し、温度が上昇することを利用したもの。
- 鉄+酸素→(熱)→酸化鉄
塩化ナトリウム活性炭などを混ぜて、丁度良い温度を保つことがように工夫してあります。
酸化カルシウムと水の反応
火を使わずに加熱できるため、携帯食品などに使われている。
- 酸化カルシウム+水→(熱)→酸化カルシウム
熱を発生する化学変化
かいろの成分を使って熱が発生する化学変化を調べます。
<手順>
- 蒸発皿に、鉄粉と活性炭をよく入れて、かき混ぜそこに食塩水を加えて混ぜる。
- 1分ごとに温度を測定し、温度変化を記録する。
<結果>
- 食塩水を加えると温度が上昇して湯気が出る
- 温度測定の記録をグラフに表すとなめらかな右上がりになる。
<考察>
- 鉄粉が空気中の酸素と化合して、熱が発生されたと考えられます。
吸熱反応
吸熱反応は、熱を吸収する化学変化。
アンモニア発生させる反応
塩化アンモニウムと水酸化バリウムに水を加える
- 水酸化バリウム+塩化アンモニウム→(熱)→塩化バリウム+アンモニア水
二酸化炭素を発生させる反応
レモン汁(クエン酸)に炭酸水素ナトリウムを加える。
反応熱
化学変化に、ともない出入りする熱。一般に化学変化では必ず熱の出入りがあります。燃焼熱、中和熱、溶解熱などがあります。
燃焼熱
物質の燃焼にともなって発生する熱量のことである。燃焼は、代表的な発熱反応である。現在の都市ガスの主成分であるメタン(CH4)1gが燃焼すると、20°Cの水160gを沸騰させることができるほどの燃焼熱が発生する。
中和熱
うすい水酸化ナトリウム水溶液にうすい塩酸を滴下していくと、ちょうど中和したときにもっとも温度が高くなる。
溶解熱
物質の溶解にともなう熱量のことである。
- 発熱反応…硫酸や水酸化ナトリウムを水に溶解させると、多量の発熱が観察される。
- 吸熱反応…硝酸アンモニウム、尿素などを水に溶解させると、温度が低下するのが観察される。
そのほかの反応熱
- 鉄の酸化…鉄粉と活性炭を混合し、これに食塩水を加えると、鉄が酸化され、熱が発生する。
- アンモニアの発生…水酸化バリウムに塩化アンモニウムを加えると、アンモニアが発生し、熱を吸収する。
- 生石灰と水の反応…生石灰(酸化カルシウム) に水を加えると激しく発熱して、水酸化カルシウムCa(OH)2。を生じる。
日常生活の中での活用
- 市販の瞬間冷却パック…水が入ったふくろと硝酸アンモニウムや尿素の粉末が入っており、水が入ったふくろを破ると、これらの物質の溶解熱のために冷却される。
- 市販の化学カイロ(使い捨てカイロ)…鉄の酸化を利用している。
熱を吸収する化学変化
アンモニアの発生で熱を吸収する化学変化を調べる実験です。
<手順>
- 試験管に塩化アンモニウムと水酸化バリウムを瓶に入れ、そこに水を加えてアンモニアを発生させる。
- フェノールフタレイン液を染み込ませた脱脂綿ですばやくふたをし、温度変化を観察する。
<結果>
- 特有の匂いがして、脱脂綿が赤色に変色し、温度が下がる。
<考察>
- アンモニアが発生して周囲の熱が吸収したことがわかる。
まとめ
- 発熱反応…熱を発生する反応(化学変化)。
- 化学かいろ…鉄が水や酸素と反応すると熱が発生し、温度が上昇することを利用したかいろ。
- 活性炭…空気中の酸素吸着するはたらき。食塩は、鉄に起こる酸化を促進するはたらきをしている。
- 吸熱反応…周囲の熱を吸収する反応(化学変化)。
- アンモニア発生させる反応…塩化アンモニウムと水酸化バリウムの粉末を混ぜ合わせる。ろ過の水にアンモニア溶けて、においが少なくなる。


コメント